

細胞死亡新方式 | 銅死亡
(1) 銅離子在細胞生理過程中的重要作用
細胞死亡是一種正常的生命現象,其相關研究一直是生命科學領域的熱點。與鐵相似,銅也是所有生物體內不可缺少的一種微量元素,在常規的化學反應和生理條件下,還原型Cu+可轉變為氧化型Cu2+。銅離子可與多種蛋白質或酶結合,作為輔助因子或結構組成部分,參與調控能量代謝、線粒體呼吸和抗氧化等多個生理過程。
(2)銅死亡(Cuproptosis):一種新型受控性細胞死亡機制
2022年3月在《Science》上發表題為Copper induces cell death by targeting lipoylated TCA cycle proteins的文章中,研究人員將一種發生機制明顯區別于已知的細胞凋亡、細胞焦亡及鐵死亡的受控性細胞死亡方式,命名為“銅死亡”(Cuproptosis)。研究人員發現銅死亡依賴于線粒體呼吸--銅離子通過直接結合三羧酸循環途徑中的硫辛酰化蛋白,導致硫辛酰化蛋白異常聚集,并干擾呼吸鏈復合體中的鐵硫簇蛋白,進而引發蛋白質毒性應激,最終致使細胞死亡。
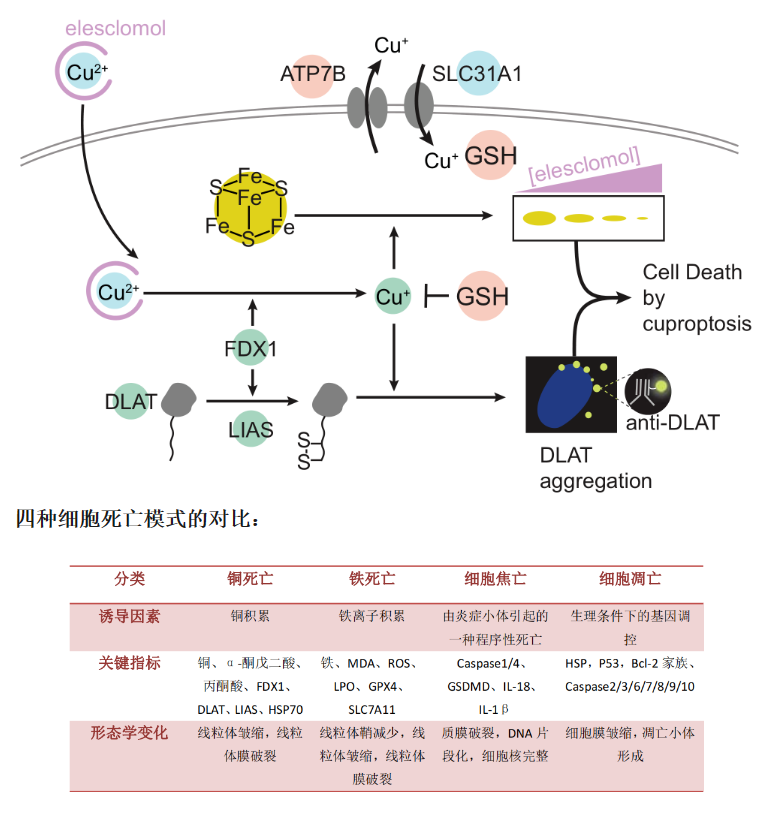
(3)10個與銅死亡相關的基因?
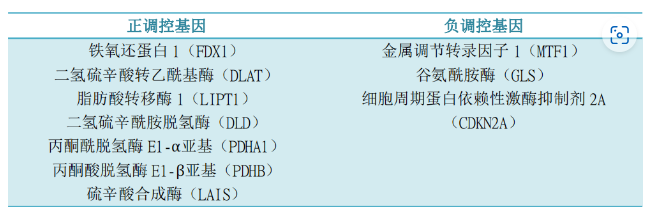
?1.線粒體呼吸調節銅離子載體誘導的細胞死亡研究發現,用銅離子載體處理不會顯著降低基礎呼吸或ATP相關呼吸,但會顯著降低呼吸的儲備能力,這表明銅不直接靶向ETC,而是靶向TCA循環的組成部分。
2.銅死亡的關鍵調控基因FDX1,是蛋白質脂化的上游調節因子為了確定介導銅毒性的特定代謝途徑,研究者通過CRISPR基因敲除篩選發現,敲除FDX1會減弱銅離子載體誘導的細胞死亡。
3.銅直接結合并誘導脂酰化DLAT的寡聚化蛋白質的硫辛酰化修飾是結合銅的必要條件。銅與硫辛酰化蛋白 DLAT 的結合,會導致蛋白的寡聚化,而 Elesclomol 處理會增加 DLAT 蛋白的寡聚化。
(4)銅催化氧化應激
-
銅介導Fenton反應催化合成最活躍的羥基自由基,從而導致細胞中的ROS濃度升高,導致細胞死亡。此外銅可以將還原的谷胱甘肽氧化成氧化型谷胱甘肽二硫物(oxidizedglutathionedisulfide,GSSG),導致抗氧化劑谷胱甘肽的耗竭,從而干擾谷胱甘肽相關的抗氧化防御系統,由此導致細胞死亡。
-
研究表明銅螯合劑伊利司莫(Elesclomol,ES),一種高度親脂性的銅結合分子,它可以螯合細胞外的Cu2+,形成一種以ES-Cu2+復合物的形式,將銅輸送到線粒體中產生氧化應激從而觸發細胞凋亡。

?(5)銅死亡在腫瘤中的相關研究
銅離子的含量維持動態平衡,失衡可導致氧化應激和細胞自噬異常等,從而誘發多種銅或銅離子相關性疾病的發生。
-
乳腺癌 有研究表明乳腺癌患者血清中Cu2+含量高于正常人。乳腺癌線粒體中銅伴侶蛋白COX17和SCO2表達上調,這說明乳腺癌細胞比正常細胞對銅向線粒體運輸的需求更高。
-
結直腸癌 銅與腫瘤微環境中的炎癥因子相互作用,炎癥因子IL-17通過誘導STEAP4來推動細胞對銅的攝取,從而促進了結直腸癌的發生。因此細胞銅代謝狀態可能是癌細胞對IL-17刺激反應的關鍵因素。
-
肺癌 有研究表明生理濃度的Cu2+聯合Disulfiram對非小細胞肺癌細胞有選擇毒性。
-
參考文獻:
[1] Tsvetkov P, Coy S, Petrova B, et al. Copper induces cell death by targeting lipoylated TCA cycle proteins. Science. 2022;375(6586):1254-1261.
-
在線咨詢
Online consultation
-
在線咨詢
-
技術支持

關注微信公眾號




